Humanos no habría existido sin virus porque la proteína viral juega un papel clave en el desarrollo de humana embrión. Sin embargo, a veces plantean amenazas existenciales en forma de enfermedades, como en el caso de la actual pandemia de COVID-19. Irónicamente, virus comprenden ~8% de nuestro genoma, que ha sido adquirido durante el curso de la evolución, lo que nos convierte en “prácticamente una quimera”.
La palabra más infame y espantosa del año 2020 sin duda es 'virus'. La novela coronavirus es responsable de la actual enfermedad COVID-19 sin precedentes y de un casi colapso de la economía mundial. Todo esto es causado por una pequeña partícula que ni siquiera se considera "plenamente" viva porque se encuentra en un estado no funcional fuera del anfitrión, mientras que solo se perpetúa en el interior al infectar al anfitrión. Más sorprendente e impactante es el hecho de que los seres humanos. han sido portadores de los “genes” virales desde tiempos inmemoriales y actualmente los genes virales constituyen ~8% de los humana genoma (1). Sólo para poner esto en perspectiva, sólo ~1% humana El genoma es funcionalmente activo responsable de producir proteínas que determinan quiénes somos.
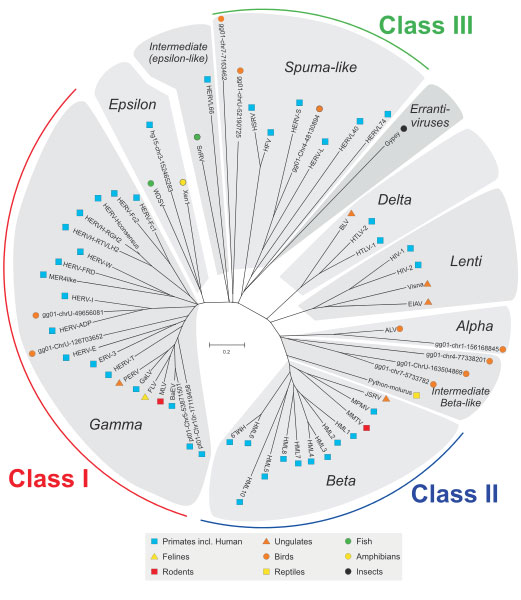
La historia de la relación entre los seres humanos. y virus comenzó hace 20-100 millones de años cuando nuestros antepasados fueron infectados por virus. Cada familia de retrovirus endógenos deriva de una única infección de las células de la línea germinal por un retrovirus exógeno que, tras integrarse en nuestro ancestro, se expandió y evolucionó (2). La propagación fue seguida por la transferencia horizontal de padres a hijos y hoy tenemos estos genomas virales incrustados en nuestro ADN como humana retrovirus endógenos (HERV). Este es un proceso continuo y puede que incluso esté ocurriendo en este momento. A lo largo de la evolución, estos HERV adquirieron mutaciones, se estabilizaron en el humana genoma y perdieron su capacidad de causar la enfermedad. lo endógeno retrovirus no sólo están presentes en los seres humanos. pero están omnipresentes en todos los organismos vivos. Todos estos retrovirus endógenos agrupados en tres clases (Clase I, II y III) que se encuentran en diferentes especies animales exhiben una relación filogenética basada en su similitud de secuencia (3), como se muestra en la Figura siguiente. Los HERV pertenecen al grupo Clase I.
De los diversos retrovirus incrustados presentes en el humana genoma, un ejemplo clásico que vale la pena mencionar aquí, es el de una proteína retroviral que es una proteína de envoltura altamente fusogénica llamada sincitina, (5) cuya función original en el virus era fusionarse con las células huésped para causar infección. Esta proteína ahora ha sido adaptada en los seres humanos. para formar placenta (fusión de células para formar células multinucleadas) que no solo proporciona alimento al feto de la madre durante el embarazo sino que también protege al feto del sistema inmunológico de la madre debido a la naturaleza inmunosupresora de la proteína sincitina. Este HERV en particular ha demostrado ser beneficioso para el humana raza definiendo su existencia misma.
Los HERV también han sido implicados en proporcionar inmunidad innata al huésped al prevenir una mayor infección por enfermedades relacionadas. virus o reducir la gravedad de la enfermedad en caso de reinfección por un tipo similar de virus. Una revisión de 2016 realizada por Katzourakis y Aswad (6) describe que endógeno virus pueden actuar como elementos reguladores de genes que controlan la función inmune, lo que conduce al desarrollo de la inmunidad. Ese mismo año, Chuong et al (7) demostraron que ciertos HERV actúan como potenciadores reguladores al modular la expresión de genes inducibles por IFN (interferón), proporcionando así inmunidad innata. Los productos de expresión de HERV también pueden actuar como patrones moleculares asociados a patógenos (PAMP), activando los receptores celulares responsables de la primera línea de defensas del huésped (8-10).
Otro aspecto interesante de los HERV es que algunos de ellos muestran polimorfismos de inserción, es decir, hay un número diferente de copias presentes en el genoma debido a eventos de inserción. Un estudio de 20 sujetos pertenecientes a diferentes grupos étnicos reveló patrones de polimorfismo de inserción entre 0-87% en todos los sujetos (11). Esto puede tener implicaciones a la hora de causar enfermedades mediante la activación de ciertos genes que, de otro modo, serían silenciosos.
También se ha demostrado que ciertos HERV están asociados con el desarrollo de trastornos autoinmunes como la esclerosis múltiple (12). En condiciones fisiológicas normales, la expresión de HERV está estrictamente regulada, mientras que en condiciones patológicas debido a cambios en el entorno externo / interno, los cambios hormonales y / o la interacción microbiana pueden causar una desregulación de la expresión de HERV, lo que conduce a la enfermedad.
Las características anteriores de los HERV sugieren que no sólo su presencia en humana El genoma es inevitable, pero poseen la capacidad de regular la homeostasis del sistema inmunológico, ya sea activándolo o suprimiéndolo, causando así efectos diferenciales (desde ser beneficiosos hasta causar una enfermedad) en los huéspedes.
La pandemia de COVID-19 también está causada por un retrovirus SARS-nCoV-2, que pertenece a la familia de la gripe, y puede ser plausible que, durante el curso de la evolución, se hayan eliminado genomas relacionados con esta familia de virus se integró en el humana genoma y ahora están presentes como HERV. Se supone que estos HERV podrían exhibir diferentes polimorfismos, como se mencionó anteriormente, entre personas de diferentes etnias. Estos polimorfismos pueden presentarse en forma de número de copias diferencial de estos HERV y/o presencia o ausencia de mutaciones (cambios en la secuencia del genoma) acumuladas durante un período de tiempo. Esta variabilidad en los HERV integrados puede ofrecer una explicación de las tasas de mortalidad diferenciales y la gravedad de la enfermedad COVID-19 en diferentes países afectados por la pandemia.
***
Referencias:
1. Griffiths DJ 2001. Retrovirus endógenos en el humana secuencia del genoma. Genoma Biol. (2001); 2(6) Reseñas 1017. DOI: https://doi.org/10.1186/gb-2001-2-6-reviews1017
2. Boeke, JD; Stoye, JP (1997). "Retrotransposones, retrovirus endógenos y la evolución de retroelementos". En Coffin, JM; Hughes, SH; Varmus, HE (eds.). Retrovirus. Prensa de laboratorio de Cold Spring Harbor. PMID 21433351.
3. Vargiu L, et al. Clasificación y caracterización de humana retrovirus endógenos; Las formas de mosaico son comunes. Retrovirología (2016); 13: 7. DOI: 10.1186 / s12977-015-0232-y
4. Classes_of_ERVs.jpg: Jern P, Sperber GO, Blomberg J (trabajo derivado: Fgrammen (charla)), 2010. Disponible en línea en https://commons.wikimedia.org/wiki/File:Classes_of_ERVs.svg Consultado el 07 de mayo de 2020.
5. Rubio, JL; Lavillette, D; Cheynet, V; Bouton, O; Oriol, G; Capilla-Fernandes, S; Mandrandés, S; Mazo, F; Cosset, FL (7 de abril de 2000). “Una glicoproteína de la envoltura del humana endógeno retrovirus HERV-W se expresa en la placenta humana y fusiona células que expresan el receptor de retrovirus de mamíferos tipo D”. J. Virol. 74 (7): 3321–9. DOI: https://doi.org/10.1128/jvi.74.7.3321-3329.2000.
6. Katzourakis A y Aswad A. Evolución: endógena Los virus Proporcionar atajos en la inmunidad antiviral. Biología actual (2016). 26: R427-R429. http://dx.doi.org/10.1016/j.cub.2016.03.072
7. Chuong EB, Elde NC y Feschotte C. Evolución reguladora de la inmunidad innata a través de la cooptación de retrovirus endógenos. Ciencia (2016) Vol. 351, número 6277, págs. 1083-1087. DOI: https://doi.org/10.1126/science.aad5497
8. Wolff F, Leisch M, Greil R, Risch A, Pleyer L. La espada de doble filo de la (re) expresión de genes mediante agentes hipometilantes: desde la mimetización viral hasta la explotación como agentes de cebado para la modulación de puntos de control inmunitarios dirigidos. Señal de comunicación celular (2017) 15:13. DOI: https://doi.org/10.1186/s12964-017-0168-z
9. Hurst TP, Magiorkinis G. Activación de la respuesta inmune innata por endógeno retrovirus. J Gen Virol. (2015) 96:1207–1218. DOI: https://doi.org/10.1099/vir.0.000017
10. Chiappinelli KB, Strissel PL, Desrichard A, Chan TA, Baylin SB, Correspondence S. La inhibición de la metilación del ADN provoca una respuesta de interferón en el cáncer mediante dsRNA que incluye retrovirus endógenos. Cell (2015) 162: 974–986. DOI: https://doi.org/10.1016/j.cell.2015.07.011
11. Mehrab G, Sibel Y, Kaniye S, Sevgi M y Nermin G. Endógeno humano retrovirus-Cribado de inserción H. Informes de medicina molecular (2013). DOI: https://doi.org/10.3892/mmr.2013.1295
12. Gröger V y Cynis H. Retrovirus endógenos humanos y su supuesta función en el desarrollo de trastornos autoinmunes como la esclerosis múltiple. Microbiol frontal. (2018); 9: 265. DOI: https://doi.org/10.3389/fmicb.2018.00265
***