Rezdiffra (resmetirom) ha sido aprobado por la FDA de EE. UU. para el tratamiento de adultos con esteatohepatitis no alcohólica no cirrótica (NASH) con cicatrización hepática (fibrosis) de moderada a avanzada, para usarse junto con dieta y ejercicio.
Hasta ahora, los pacientes con esteatohepatitis no alcohólica no cirrótica (NASH, por sus siglas en inglés) que también tienen cicatrices hepáticas notables no tenían un medicamento que pudiera abordar directamente su problema. Daño hepático. FDA La aprobación de Rezdiffra proporcionará, por primera vez, una opción de tratamiento para estos pacientes, además de dieta y ejercicio.
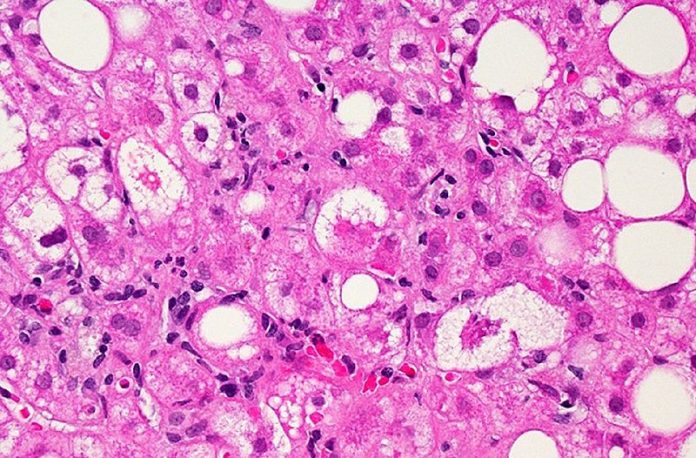
NASH es el resultado de la progresión de grasas no alcohólicas. hígado enfermedades donde hígado La inflamación, con el tiempo, puede provocar cicatrices en el hígado y disfunción hepática. NASH a menudo se asocia con otros problemas de salud como presión arterial alta y diabetes tipo 2. Según al menos una estimación, aproximadamente entre 6 y 8 millones de personas en los EE. UU. tienen NASH con cicatrización hepática de moderada a avanzada, y se espera que ese número aumente.
Rezdiffra es un activador parcial del receptor de la hormona tiroidea; La activación de este receptor por parte de Rezdiffra en el hígado reduce la acumulación de grasa en el hígado.
Seguridad y eficacia de Rezdiffra
La seguridad y eficacia de Rezdiffra se evaluaron basándose en un análisis de un criterio de valoración sustituto en el mes 12 en un ensayo aleatorizado, doble ciego y controlado con placebo de 54 meses de duración. El criterio de valoración sustituto midió el alcance de hígado inflamación y cicatrización. El patrocinador debe realizar un estudio posterior a la aprobación para verificar y describir el beneficio clínico de Rezdiffra, lo que se realizará completando el mismo estudio de 54 meses, que aún está en curso. Para inscribirse en el ensayo, los pacientes debían tener una hígado biopsia que muestra inflamación debido a NASH con moderada o avanzada hígado cicatrización. En el ensayo, 888 sujetos fueron asignados aleatoriamente para recibir uno de los siguientes: placebo (294 sujetos); 80 miligramos de Rezdiffra (298 sujetos); o 100 miligramos de Rezdiffra (296 sujetos); una vez al día, además de la atención estándar para NASH, que incluye asesoramiento sobre una dieta saludable y ejercicio.
A los 12 meses, las biopsias de hígado mostraron que una mayor proporción de sujetos que fueron tratados con Rezdiffra lograron una resolución de NASH o una mejora en la cicatrización del hígado en comparación con aquellos que recibieron el placebo. Un total del 26 % al 27 % de los sujetos que recibieron 80 miligramos de Rezdiffra y del 24 % al 36 % de los sujetos que recibieron 100 miligramos de Rezdiffra experimentaron una resolución de la EHNA y ningún empeoramiento de las cicatrices hepáticas, en comparación con el 9 % al 13 % de los que recibieron recibieron placebo y asesoramiento sobre dieta y ejercicio. La variedad de respuestas refleja las lecturas de diferentes patólogos. Además, un total del 23% de los sujetos que recibieron 80 miligramos de Rezdiffra y del 24% al 28% de los sujetos que recibieron 100 miligramos de Rezdiffra experimentaron una mejora en hígado cicatrices y ningún empeoramiento de NASH, en comparación con el 13% al 15% de los que recibieron placebo, dependiendo de las lecturas de cada patólogo. Es notable la demostración de estos cambios en una proporción de pacientes después de sólo un año de tratamiento, ya que la enfermedades Por lo general, progresa lentamente y la mayoría de los pacientes tardan años o incluso décadas en mostrar progresión.
Efectos secundarios de Rezdiffra
Los efectos secundarios más comunes de Rezdiffra incluyeron diarrea y náuseas. Rezdiffra viene con ciertas advertencias y precauciones, como toxicidad hepática inducida por medicamentos y efectos secundarios relacionados con la vesícula biliar.
Se debe evitar el uso de Rezdiffra en pacientes con cirrosis descompensada. Los pacientes deben dejar de usar Rezdiffra si desarrollan signos o síntomas de empeoramiento. hígado funcionar durante el tratamiento con Rezdiffra.
Interacciones farmacológicas de Rezdiffra
El uso de Rezdiffra al mismo tiempo que otros medicamentos, en particular estatinas para reducir el colesterol, puede provocar interacciones medicamentosas potencialmente significativas. Los proveedores de atención médica deben consultar la información de prescripción completa para obtener información adicional sobre estas interacciones medicamentosas potencialmente significativas con Rezdiffra, la dosis recomendada y las modificaciones de la administración.
La FDA aprobó Rezdiffra bajo la vía de aprobación acelerada, que permite la aprobación temprana de medicamentos que tratan enfermedades graves y abordan una necesidad médica no cubierta, basándose en un criterio de valoración clínico sustituto o intermedio que tenga una probabilidad razonable de predecir el beneficio clínico. El estudio requerido de 54 meses de duración, que está en curso, evaluará el beneficio clínico después de 54 meses de tratamiento con Rezdiffra.
Rezdiffra recibió las designaciones de Terapia Innovadora, Vía Rápida y Revisión Prioritaria para esta indicación.
La FDA concedió la aprobación de Rezdiffra a Madrigal Pharmaceuticals.
***
Fuente:
FDA 2024. Comunicado de prensa: La FDA aprueba el primer tratamiento para pacientes con cicatrices hepáticas debido a la enfermedad del hígado graso. Publicado el 14 de marzo de 2024. Disponible en https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
***